(1)黑龙江省自然科学基金面上项目,LH2022C071,冷诱导的组蛋白乳酸化对猪肺泡巨噬细胞免疫活性调控机制的研究,在研,主持.
(2)黑龙江省博士后科研启动基金,LBH-Q20163,lncRNA NONRATT021477.2在大鼠肝脏氧化应激调控中的作用及机制,在研,主持.
技术指导和经费支持
(1)黑龙江省自然科学基金面上项目,LH2022C071,冷诱导的组蛋白乳酸化对猪肺泡巨噬细胞免疫活性调控机制的研究,在研,主持.
(2)黑龙江省博士后科研启动基金,LBH-Q20163,lncRNA NONRATT021477.2在大鼠肝脏氧化应激调控中的作用及机制,在研,主持.
技术指导和经费支持
| 序号 | 学生 | 所属学院 | 专业 | 年级 | 项目中的分工 | 成员类型 |
|---|---|---|---|---|---|---|
|
|
李梦涵 | 动物科技学院 | 动物医学(创新人才班) | 2021 | 血液和肝脏指标检测 |
|
|
|
陈多思 | 动物科技学院 | 动物医学(创新人才班) | 2022 | 小鼠生长性能指标检测 |
|
|
|
阚兴旭 | 动物科技学院 | 动物科学 | 2022 | 小鼠饲喂及灌胃操作 |
|
|
|
李子怡 | 动物科技学院 | 动物医学(创新人才班) | 2021 | 组织切片制备 |
|
|
|
朱亚鑫 | 动物科技学院 | 动物医学(创新人才班) | 2022 | 小鼠模型构建及样品采集 |
|
| 序号 | 教师姓名 | 所属学院 | 是否企业导师 | 教师类型 |
|---|---|---|---|---|
|
|
计红 | 动物科技学院 | 否 |
|
在寒冷地区,环境低温是制约动物健康和动物生产的主要因素之一。寒冷可导致动物机体发生冷应激,引起畜禽生理机能紊乱,代谢异常,免疫力降低,严重影响畜禽福利以及我国规模化养殖的生产。肝脏是机体新陈代谢的重要器官,本实验室前期研究显示,冷刺激可导致肝脏发生损伤。桑色素是一种具有多重生物活性的多酚类物质,具有抗氧化、降血糖、抗炎、抑制酶活性、抗癌、抑菌、抗动脉粥样硬化等功效,且其毒性非常低。桑色素对冷应激诱导的小鼠肝脏发生的氧化应激和组织损伤具有怎样的调控作用,目前尚不明确。因此本课题以小鼠为研究对象,以冷暴露为基本处理方法,研究在饲粮中添加不同剂量桑色素对冷应激小鼠生长性能、肝脏组织形态学结构及氧化损伤的影响,探讨桑色素对小鼠冷应激肝脏损伤的改善作用,为开发应用桑色素作为一种天然的绿色饲料添加剂提供理论基础和参考。
1.动物分组及模型构建
将30只C57BL/6小鼠分为6组,每组5只,分别为常温对照组(C组)、冷刺激组(CS组)、桑色素对照组(M组)、冷刺激+低剂量桑色素治疗组(CS+ML组)、冷刺激+中剂量桑色素治疗组(CS+MM组)、冷刺激+高剂量桑色素治疗组(CS+MH组)。桑色素的给药方式采取灌胃给药。根据各组小鼠数量用天平称取所需桑色素剂量并用对应体积的PBS缓冲液进行溶解,然后分别进行灌胃给药。其中C组和CS组则给予等体积的PBS缓冲液。
根据实验室前期研究基础,将小鼠置于4℃人工智能气候室中进行冷刺激处理。小鼠灌胃给药1 h后,除C组和M组小鼠仍每天保持在24±2℃环境中饲养,其余组小鼠则每天被置于4℃环境中随机进行冷刺激3 h,持续3周。造模结束后,麻醉各组小鼠,进行眼球采血并分离血清,存放于-80℃冰箱待用;采取肝脏样品置于液氮待用。
2.小鼠生长指标的测定
实验开始的第1日规定时间和饲料量,每日早8点进行饲喂,先称量昨日所剩饲料量,再称量当日所需饲料量。平均日采食量(g/d)=实验期总采食量/实验周期。同样以实验开始的第一日规定时间,例如以第一日早8点的小鼠体重作为初始体重,以后每周称量1次,造模结束当日早8点的小鼠体重作为末始体重。平均日增重(g/d)=(末始体重-初始体重)/实验周期。将采取的内脏器官上面的结缔组织及脂肪组织剔除后称重并计算。脏器指数(mg/g)=脏器重量/小鼠体重。
3.病理组织切片的制作及肝脏损伤评分
将置于4%多聚甲醛固定的肝脏样品取出,然后放入梯度乙醇中进行脱水,再用二甲苯溶液浸泡透明。将脱水透明后的样品进行浸蜡包埋,待凝固后切成3-4μM的薄片。烘干、脱蜡、水化后进行HE染色,再使用中性树胶封片,最后用光学显微镜观察拍照。采用半定量评分系统评估肝损伤,具体病理分级的评分标准见表1。将每一评分累加即得到评估肝损伤严重程度的评分。
表1肝脏组织损伤评分标准
项目 | 程度 | 评分 |
肝索界限清晰程度 | 界限清晰 | 0 |
界限不清晰 | 1 | |
肝细胞变性程度 | 无 | 0 |
轻度(肝细胞轻微颗粒变性) | 1 | |
中度(肝细胞大量颗粒变性,并伴随少量空泡变性) | 2 | |
重度(肝细胞大量空泡变性) | 3 | |
肝脏炎性细胞浸润情况 | 无炎性细胞浸润 | 0 |
轻度(<5个/HP炎性细胞浸润) | 1 | |
中度(5-10个/HP炎性细胞浸润) | 2 | |
重度(>10个/HP炎性细胞浸润) | 3 | |
肝脏汇管区水肿情况 | 无 | 0 |
轻度 | 1 | |
中度 | 2 | |
重度 | 3 |
4.小鼠肝脏指标的检测
采集小鼠肝脏样品进行氧化应激相关指标的检测,具体如下:
(1)活性氧(Reactive oxygen species, ROS)检测:取各组小鼠的新鲜肝脏组织,制成冰冻切片,严格按照ROS试剂盒说明书操作完成后,使用荧光显微镜观察拍照。
(2)丙二醛(Malondialdehyde, MDA)含量的检测:从-80℃冰箱中取出小鼠肝脏样品,准确称取样品重量,按重量(g):体积(mL)=1:9的比例加入PBS溶液,用球磨仪研磨,制备成10%的组织匀浆,12000 r/min,4°C离心10 min,取上清,置于冰上待检。严格按照试剂盒操作步骤进行检测。
(3)谷胱甘肽(Glutathione, GSH)含量的检测:将肝组织匀浆,方法同“MDA检测”,严格按照GSH试剂盒操作步骤进行检测。
(4)超氧化物歧化酶(Superoxide dismutase, SOD)活性的检测:将肝组织匀浆,方法同“MDA检测”,严格按照MDA试剂盒操作步骤进行检测。
(5)过氧化氢酶(Catalase, CAT)活性的检测:将肝组织匀浆,方法同“MDA检测”,严格按照CAT活性检测试剂盒说明书进行检测。
(6)谷胱甘肽过氧化物酶(Glutathione Peroxidase, GSH-Px)活性的检测:将肝组织匀浆,方法同“MDA检测”,严格按照GSH-Px活性检测试剂盒说明书进行检测。
(7)总抗氧化能力(Totalantioxidantcapacity, TAOC)水平的测定:将肝组织匀浆,方法同“MDA检测”,严格按照T-AOC检测试剂盒说明书进行检测。
5.小鼠血清相关指标的测定
从-80℃冰箱中取出小鼠肝脏样品,称取约0.1 g肝脏组织,加入1 mL提取液进行冰浴匀浆。8000 r/min,4℃离心10 min,取上清,置冰上待测。采用试剂盒对血清样本谷丙转氨酶(Alanine transaminase, ALT)与谷草转氨酶(Aspartate transaminase, AST)进行检测。
1936年,病理学家Hans Selye首次提出了“应激学说”,阐明应激是指动物机体受到内外环境、社会及心理因素刺激时所出现的全身性、非特异性适应反应。而由应激引起的这些非特异性反应又称为“全身适应综合征”(General adaptation syndrome, GAS),能引起机体出现GAS的刺激源则被称为“应激源”[1]。应激可使交感神经兴奋,促进垂体和肾上腺皮质分泌的激素增多,升高血糖和血压,加快心率和呼吸,且使机体代谢异常,持续一定程度的应激可使机体患病甚至死亡[2]。引起动物应激的因素丰富多样,如环境骤变、长途运输、缺氧、惊吓、创伤等[3],这些应激源所导致的反应不仅损害了动物福利,也限制了畜牧业的发展。
环境低温是制约我国寒区畜牧业发展的主要应激源之一。冷应激通常是指对温度突然骤降(温差大于10℃)的环境刺激或是长期处于低温环境下(4℃以下)所产生的一系列生理或病理反应,既有抗损伤反应的产生,也有病理损伤的出现,关键取决于冷应激反应的强弱和机体对冷应激的适应性。短时间的低温刺激能够使机体交感神经兴奋并增强代谢;但较长时间处于低温环境中,会导致机体运动神经和感觉神经的功能受到抑制,严重时可对机体造成不可逆的损害[4]。
内脏器官是动物生理功能的基础,而脏器的质量及指数能准确反映出动物对环境的适应情况[5]。由于冷应激极易诱导机体内脏器官发生水肿,因此脏器质量及脏器指数会受到一定影响。陈帅[6]研究将断奶仔猪分为对照组(25-27℃)和低温组(14-16℃)进行为期21天的饲养,结果显示低温组断奶仔猪心脏、肺脏、肝脏、脾脏和肾脏的脏器指数均与对照组无显著差异。赵守彰等[7]研究指出冷应激会使小鼠肝脏和胰腺指数提高。总之,多项研究证实环境低温对动物脏器质量及指数的影响,但是针对不同品种的动物对冷应激刺激强度的适应程度也不尽相同,因此脏器指数也因个体差异及温度条件的变化呈现不同的结果。现已被证明,环境低温会诱导多种内脏器官发生病理性损伤,如组织间隙及细胞水肿,细胞变性及坏死,并伴随组织内炎性细胞浸润等。李鹏等[8]研究表明不论是急性冷暴露还是慢性冷暴露条件下均对大鼠脾脏、淋巴结、肝脏、十二指肠组织结构产生病理性损伤,具体表现为脾和淋巴结内淋巴小结减少,动脉周围淋巴鞘变薄,十二指肠粘膜上皮增厚,肝脏发生可恢复的脂肪变性等。综上表明,环境低温对机体内脏器官的影响不容小觑,能够诱导多种组织结构发生病理变化,进而造成全身性损伤。
当动物机体长期处于低温环境时,通过减少散热量已经不能维持机体稳态,因此就需要机体增加产热量以保持体温恒定。增加产热量则需要提高自身代谢水平,通过将营养物质进行氧化分解释放更多热量,在这个过程中会产生大量氧化自由基如活性氧自由基(ROS)和活性氮自由基(RNS)等,使机体中的氨基酸和脂质等多种物质受到攻击,进而对机体产生氧化损伤[9]。冷应激可诱导肝脏氧化应激的发生。臧树成[10]研究发现,冷刺激后大鼠肝脏组织内丙二醛(MDA)含量,半胱天冬蛋白酶-3(Caspase-3)和细胞色素C(Cytc)蛋白水平显著上升,并显著下降了GSH-Px活性和超氧化物歧化酶1(SOD-1)蛋白水平。Venditti等[11]研究发现,冷刺激后大鼠肝脏中能量代谢的水平提高,过氧化氢(Hydrogen peroxide, H2O2)含量显著升高,而总抗氧化能力呈下降趋势。Berrak等[12]研究了冷应激对大鼠肝、胃和血浆中谷胱甘肽和脂质过氧化物水平的影响,发现冷应激可使大鼠肝脏和胃还原型谷胱甘肽(GSH)含量显著降低。Ates等[13]研究也证实冷应激后大鼠肝脏组织中过氧化氢酶(CAT)、SOD、GSH-Px的活性及总GSH含量平均显著下降,提示冷应激可导致肝脏发生氧化应激并造成氧化损伤。
自由基是人体生命活动中生化反应的中间代谢产物,具有高度的化学活性,黄酮类物质具有还原性以及捕获自由基的特性。研究表明,桑色素可抑制γ射线所引起的胞内ROS水平的上升,保护细胞免受辐射诱导的脂质过氧化和细胞DNA损伤[14]。Zhang R等[15]研究表明桑色素对过氧化氢(H2O2)诱导的DNA和脂质损伤的功能具有抑制效应。Vanitha等[16]研究显示桑色素通过对细胞内抗氧化酶活性的增强和激活Nrf-2/抗氧化反应元件(Antioxidant response element, ARE)信号通路来保护胰腺β细胞免受氧化应激诱导的DNA损伤。Sreedharan V等[17]研究结果显示,在二甲肼(DMH)处理的大鼠中,肝脏中酶和非酶的抗氧化物的含量较低,而脂质过氧化(LPO)产物的含量较高,但是桑色素补充后可使这些指标趋于正常水平。资料也显示在体内补充桑色素通过减少APAP诱导的肝毒性的组织学和血清标志物,减弱APAP介导的肝损伤,抑制氧化应激和线粒体功能障碍[16]。这些结果提示桑色素具有一定的抗氧化作用。
补充天然抗氧化剂已被用于缓解畜禽应激。由于桑色素对畜禽应激功能的调控作用相关研究较少,桑色素对冷应激导致的机体损伤具有怎样的影响尚不完全清楚。因此本课题以小鼠为研究对象,以冷暴露为基本处理方法,研究在饲粮中添加不同剂量桑色素对冷应激小鼠生长性能、肝脏组织形态学结构及氧化损伤的影响,并探讨桑色素对仔猪冷应激肝脏损伤的改善作用及机制。本研究的结果对桑色素作为饲料添加剂对动物生长的营养调控及抗应激调控均可提供重要参考和借鉴。
参考文献:
[1]Selye H. A syndrome produced by diverse nocuous agents. 1936[J]. The Journal of Neuropsychiatry and Clinical Neurosciences, 1998, 10(2): 230-231.
[2]Yaribeygi H, Panahi Y, Sahraei H, et al. The impact of stress on body function: A review[J]. EXCLI Journal, 2017, 16: 1057-1072.
[3]Elshazly S M, Abd E l Motteleb D M, Ibrahim IAAE. Hesperidin protects against stress induced gastric ulcer through regulation of peroxisome proliferator activator receptor gamma in diabetic rats[J]. Chemico-Biological Interactions, 2018, 291: 153-161.
[4]Westfall T C, Yang C L, Chen X, et al. A novel mechanism prevents the development of hypertension during chronic cold stress[J]. Autonomic&Autacoid P0harmacology, 2005, 25(4): 171-177.
[5]张守栋,杨传华,林恭华,等. 高寒草甸3种啮齿动物内脏器官及相关性比较[J]. 四川动物, 2015, 34(03): 424-428.
[6]陈帅,低温环境对断奶仔猪生长性能和骨骼肌纤维的影响及下限温度临界值的探究[D].四川农业大学, 2019.
[7]赵守彰,张建军. 褐藻寡糖对冷应激小鼠肝脏和胰腺的影响[J]. 中国卫生标准管理,2015, 6(19): 188-190.
[8]李鹏,杨焕民,任宝波等. 冷应激大鼠几种组织形态结构变化的研究[J]. 黑龙江八一农垦大学学报,2004, 2: 51-55.
[9]姜伟. 氧化应激介导Nrf2/HO-1与JAK1/STAT3通路参与三氯乙烯致敏小鼠肝脏损伤[D]. 安徽医科大学, 2021.
[10]臧树成. miR-383在急性冷暴露诱导大鼠肝脏氧化应激中的作用[D]. 黑龙江八一农垦大学, 2019.
[11]Venditti P, Rosa R D, Portero-Otin M, et al. Cold-induced hyperthyroidism produces oxidative damage in rat tissues and increases susceptibility to oxidants[J]. International Journal of Biochemistry&Cell Biology, 2004, 36(7): 1319-1331.
[12]Berrak Y, Alpaslan D, Ilker A, et al. Effect of cold-restraint stress on glutathione and lipid peroxide levels in the liver and glandular stomach of rats[J]. Pharmacological Research, 1990, 22(1): 45-48.
[13]Ates B, Dogru M I, Gul M, et al. Protective role of caffeic acid phenethyl ester in the liver of rats exposed to cold stress[J]. Fundamental&Clinical Pharmacology, 2006, 20(3): 283-289.
[14]Zhang R,Kang K A,Kang S S, et al. Morin(2′,3,4′,5,7-Pentahydroxyflavone)protected cells againstγ-radiation-induced oxidative stress[J]. Basic and Clinical Pharmacology and Toxicology, 2011, 108(1): 63-72.
[15]Zhang R, Kang K A, Piao M J, et al. Cellular protection of morin against the oxidative stress induced by hydrogen peroxide[J]. Chemico-Biological Interactions, 2009, 177(1): 21-27.
[16]Vanitha P, Senthilkumar S, Dornadula S, et al. Morin activates the Nrf2-ARE pathway and reduces oxidative stress-induced DNA damage in pancreatic beta cells[J]. European Journal of Pharmacology: An International Journal, 2017, 801: 9-18.
[17]Kaushik S, Kaur J. Chronic cold exposure affects the antioxidant defense system in various rat tissues[J]. Clinica Chimica Acta, 2003, 333(1): 69-77.
动物冷应激机制相关研究较多,但涉及到将桑色素作为抗冷应激营养调控的添加剂的研究较少,本项目主要研究不同添加剂量桑色素对冷应激小鼠的生长性能、肝脏组织学结构和肝损伤的改善作用,在研究内容具有一定创新性。本项目具有重要实际意义,和临床冷应激防控紧密结合,并研究桑色素对畜牧生产中动物冷应激的调控作用,为研究有效缓解应激所致动物机体损伤的临床药物提供理论依据。
技术路线:
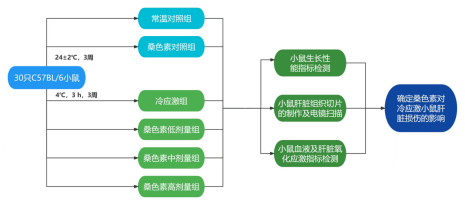
拟解决的问题:
在寒冷地区,环境低温是制约动物健康和动物生产的主要因素之一肝脏是机体重要的新陈代谢的重要器官,在慢性冷刺激作用下可发生氧化应激和肝损伤。桑色素具有抗氧化、抗炎、抗癌等多种药理活性,但其对于动物机体冷应激的调控作用研究鲜见。因此课题以小鼠为研究对象,以冷暴露为基本处理方法,研究在饲粮中添加不同剂量桑色素对冷应激小鼠生长性能、肝脏组织形态学结构及氧化损伤的影响,探讨桑色素对小鼠冷应激肝脏损伤改善作用。本研究的结果对桑色素作为饲料添加剂对仔猪生长的营养调控及抗应激调控均可提供重要参考和借鉴。
预期成果:
1.明确桑色素对冷应激小鼠生长性能及肝脏氧化损伤的调控作用。
2.申请软件著作权1
(1)2023年6月~2023年9月 参考国内外科研人员的研究成果,最终确定本实验的刺激条件以及完善实验设计。
(2)2023年10月~2023年12月 构建慢性冷暴露组及桑色素治疗组小鼠模型,采集小鼠血清及肝脏样品。测定生长指标数值。
(3)2024年1月~2024年6 月 研究桑色素对慢性冷暴露诱导小鼠肝脏组织发生的氧化应激的影响,撰写论文,申请软件著作权,撰写结题报告。
本次申请课题指导教师自2003年一直从事动物冷应激相关研究,持过国家自然科学基金青年基金、中国博士后科学基金、黑龙江省自然科学基金等项目,作为主要参加人参加过多项应激相关等课题,发表文章30余篇,其中SCI收录10篇,专著1部,教材4部,指导过国家级大创一项,这些科研经历使申请人对冷应激机制的研究有了更深入的理解,有助于对应激理论知识的凝练和总结,也形成了丰富的科研经验,同时,本项目申请人在黑龙江八一农垦大学生物技术中心学习一年,具备完成该实验的技术和能力。这些都为本项目的顺利完成提供了重要保障。
本实验拟在黑龙江八一农垦大学生物技术中心完成,中心具备开展本课题研究所需的智能人工气候室、生化分析仪,切片机等仪器设备,可保障项目的顺利实施。此外,指导教师近十几年来一直从事冷应激相关课题的研究,经验丰富,当课题遇到的困难也会得到及时沟通和解决,这些可保证本项目顺利开展。
| 开支科目 | 预算经费(元) | 主要用途 | 阶段下达经费计划(元) | |
|---|---|---|---|---|
| 前半阶段 | 后半阶段 | |||
| 预算经费总额 | 5000.00 | 无 | 3500.00 | 1500.00 |
| 1. 业务费 | 2500.00 | 无 | 1000.00 | 1500.00 |
| (1)计算、分析、测试费 | 1000.00 | 电镜扫描 | 1000.00 | 0.00 |
| (2)能源动力费 | 0.00 | 无 | 0.00 | 0.00 |
| (3)会议、差旅费 | 0.00 | 无 | 0.00 | 0.00 |
| (4)文献检索费 | 1500.00 | 软件著作权申请或者版面费 | 0.00 | 1500.00 |
| (5)论文出版费 | 0.00 | 无 | 0.00 | 0.00 |
| 2. 仪器设备购置费 | 0.00 | 无 | 0.00 | 0.00 |
| 3. 实验装置试制费 | 0.00 | 无 | 0.00 | 0.00 |
| 4. 材料费 | 2500.00 | 实验试剂及耗材 | 2500.00 | 0.00 |